Як Резерфорд установив природу α-частинок
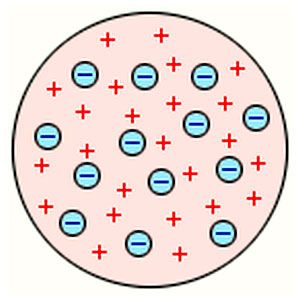
Модель атома Томсона добре описувала явище випускання катодних променів. Однак, вона нічого не говорила про розподіл заряду по атому. Для його вивчення Е. Резерфорд запропонував поставити спеціальний дослід.
Коротко про дослід Ернеста Резерфорда можна сказати наступне. Багато радіоактивних речовин випускають α-частинки, маса яких набагато більша за масу електронів, а заряд дорівнює подвоєному заряду електрона. Тепер, якщо опромінювати речовина α-частинками, то легкі електрони, що входять до складу атома, не зможуть змінити напрямок їх руху. Розсіювання α-частинок можливе лише на позитивно зарядженій частині атома.
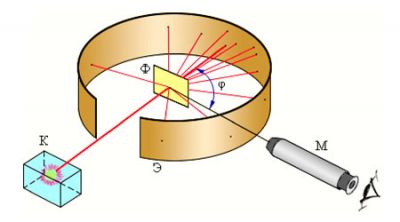
Експериментальна установка фізика складалася з контейнера з радієм, що випускає α-частинки, на шляху яких була встановлена тонка металева фольга, а за фольгою розмішувався екран, покритий сульфідом цинку, на якому при попаданні α-частинок виникало світіння (сцинтиляція). Схема експерименту представлена на наступному малюнку:
Без фольги, в точці опромінення виникала сцинтиляційна пляма. Якщо на шляху польоту α-частинок помістити фольгу – розмір плями збільшиться за рахунок розсіювання частинок через взаємодію з позитивними зарядами. За характером зміни плями можна судити про розподіл позитивного заряду в атомах речовини.
Результати досліду Ернеста Резерфорда
Якщо позитивний заряд рівномірно розподілений по речовині, розсіювання α-часток не мало відбуватись. Відповідно до моделі атома Томсона, позитивні заряди мають деяку просторову неоднорідність, а значить, розсіювання з`явиться.
Розсіювання, дійсно, з`явилося, але при цьому мало досить цікавий розподіл – деяка частина частинок відхилялася на досить помітні кути, а іноді, на багато більші, ніж була розрахована установка.
Це вже говорило про велику нерівномірність розподілу позитивного заряду. Установка була модифікована, екрани стали встановлюватися навколо неї.
І з великим подивом Резерфорд виявив, що невелике число часток (близько 0, 05%) відхиляються на дуже великі кути, більше 90⁰, а деякі – навіть «відскакували» від фольги в зворотному напрямку.
Якщо припустити, що позитивний заряд має радіус близько 10-10 м, то заряд q повинен майже в сто тисяч разів перевищувати заряд електрона. Оскільки атом нейтральний, то можна припустити, що число електронів в сто тисяч разів більший, ніж число атомів. Однак, таке число електронів мають значну масу, яка не реєструвалася під час досліду.
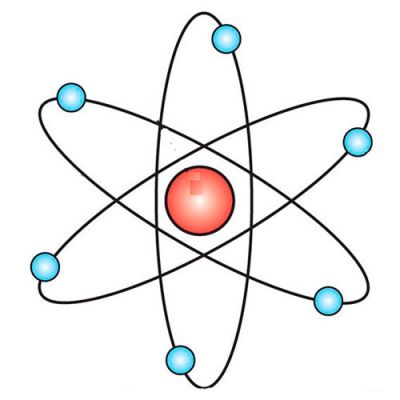
Отже, позитивний заряд зосереджений в дуже невеликій частини атома, яка була названа ядром. Розрахунки показали, що розмір ядра атома має величину порядку 10-14–10-15 м. Електрони ж рухаються навколо ядра на великій відстані. Після цього експерименту була побудована планетарна модель атома Резерфорда:
Досвід Резерфорда також дозволив оцінити і заряд ядра. Він виявився різним для різних матеріалів, і якщо прийняти за одиницю заряд електрона, то заряд ядра виявився рівним порядковому номеру елемента в періодичній системі хімічних елементів Д. І. Менделеєва.